
כל תוכן iLive נבדק מבחינה רפואית או נבדק למעשה כדי להבטיח דיוק עובדתי רב ככל האפשר.
יש לנו קווים מנחים קפדניים המקור רק קישור לאתרים מדיה מכובד, מוסדות מחקר אקדמי, בכל עת אפשרי, עמיתים מבחינה רפואית מחקרים. שים לב שהמספרים בסוגריים ([1], [2] וכו ') הם קישורים הניתנים ללחיצה למחקרים אלה.
אם אתה סבור שתוכן כלשהו שלנו אינו מדויק, לא עדכני או מפוקפק אחרת, בחר אותו ולחץ על Ctrl + Enter.
חיסון סינתטי מורכב המבוסס על מולקולות DNA נוצר
המומחה הרפואי של המאמר
סקירה אחרונה: 01.07.2025
בחיפוש אחר דרכים ליצור חיסונים בטוחים ויעילים יותר, מדענים במכון Biodesign באוניברסיטת אריזונה סטייט פנו לתחום מבטיח בשם ננוטכנולוגיה של DNA כדי ליצור סוג חדש לגמרי של חיסון סינתטי.
במחקר שפורסם לאחרונה בכתב העת Nano Letters, האימונולוג יונג צ'אנג מהמכון לביו-הנדסה חברה לעמיתים, ביניהם ננו-טכנולוג ה-DNA הנודע האו יאן, כדי לסנתז את קומפלקס החיסונים הראשון בעולם שניתן להעבירו בבטחה וביעילות לאתרי מטרה על ידי הצבתו על ננו-מבנים תלת-ממדיים של DNA המתאספים מעצמם.
"כאשר האו הציע שנראה את ה-DNA לא כחומר גנטי אלא כפלטפורמת עבודה, עלה לי הרעיון ליישם גישה זו באימונולוגיה", אומר צ'אנג, פרופסור חבר בבית הספר למדעי החיים וחוקר במרכז למחלות זיהומיות וחיסונים במכון להנדסה ביולוגית. "זה ייתן לנו הזדמנות מצוינת להשתמש בנשאי DNA כדי ליצור חיסון סינתטי."
"השאלה הגדולה הייתה: האם זה בטוח? רצינו ליצור קבוצת מולקולות שיכולות לעורר תגובה חיסונית בטוחה וחזקה בגוף. מאחר שצוותו של האו עיצב ננו-מבנים שונים של DNA בשנים האחרונות, התחלנו לשתף פעולה כדי למצוא יישומים רפואיים פוטנציאליים למבנים אלה."
ייחודה של השיטה שהוצעה על ידי מדענים מאריזונה הוא שנשא האנטיגן הוא מולקולת DNA.
צוות המחקר הרב-תחומי כלל גם את סטודנט לתואר שני בביוכימיה מאוניברסיטת אריזונה והמחבר הראשון של המאמר שיאוווי ליו, פרופסור יאנג שו, מרצה לביוכימיה יאן ליו, סטודנט בבית הספר למדעי החיים קרייג קליפורד וטאו יו, סטודנט לתואר שני מאוניברסיטת סצ'ואן בסין.
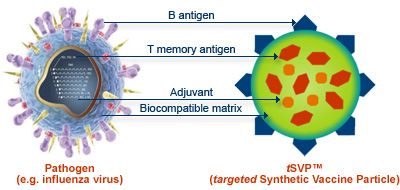
צ'אנג מציין כי האימוץ הנרחב של חיסונים הוביל לאחד הניצחונות המשמעותיים ביותר של בריאות הציבור. אמנות יצירת החיסונים מסתמכת על הנדסה גנטית לבניית חלקיקים דמויי וירוס מחלבונים המגרים את מערכת החיסון. חלקיקים אלה דומים במבנה שלהם לווירוסים אמיתיים אך אינם מכילים רכיבים גנטיים מסוכנים הגורמים למחלות.
יתרון חשוב של ננוטכנולוגיה של DNA, המאפשרת לתת למולקולה ביולוגית צורה דו-ממדית או תלת-ממדית, הוא היכולת ליצור מולקולות באמצעות שיטות מדויקות מאוד שיכולות לבצע פונקציות אופייניות למולקולות טבעיות בגוף.
"ערכנו ניסויים בגדלים וצורות שונים של ננו-מבנים של DNA והוספנו להן ביו-מולקולות כדי לראות כיצד הגוף יגיב", מסביר יאנג, מנהל המחלקה לכימיה וביוכימיה וחוקר במרכז לביופיזיקה של מולקולות בודדות במכון להנדסה ביולוגית. באמצעות גישה שהמדענים מכנים "ביומימיקרי", קומפלקסי החיסונים שבדקו קרובים לגודל ולצורה של חלקיקי וירוס טבעיים.
כדי להדגים את כדאיות הקונספט שלהם, החוקרים חיברו את החלבון סטרפטבידין (STV) המעורר את מערכת החיסון ואת התרופה CpG אוליגודיאוקסינוקלאוטיד המחזקת את מערכת החיסון למבני DNA מסועפים פירמידליים נפרדים, מה שאפשר להם בסופו של דבר להשיג קומפלקס חיסון סינתטי.
ראשית, הצוות היה צריך להוכיח שתאי המטרה יכולים לספוג את הננו-מבנים. על ידי חיבור מולקולת תג פולטת אור לננו-מבנה, המדענים הצליחו לוודא שהננו-מבנה מצא את מקומו המתאים בתא ונשאר יציב במשך מספר שעות - מספיק זמן כדי לעורר תגובה חיסונית.
לאחר מכן, בניסויים על עכברים, המדענים עבדו על העברת "מטען" החיסון לתאים שהם החוליה הראשונה בשרשרת התגובה החיסונית של הגוף, תוך תיאום אינטראקציות בין רכיבים שונים כגון תאים מציגי אנטיגן, כולל מקרופאגים, תאים דנדריטים ותאי B. לאחר שהננו-מבנים נכנסים לתא, הם "מנותחים" ו"מוצגים" על פני התא כך שניתן יהיה לזהות אותם על ידי תאי T, תאי הדם הלבנים הממלאים תפקיד מרכזי בהפעלת תגובת ההגנה של הגוף. תאי T, בתורם, מסייעים לתאי B לייצר נוגדנים כנגד אנטיגנים זרים.
כדי לבדוק באופן מהימן את כל הווריאנטים, החוקרים הזריקו לתאים הן את קומפלקס החיסון המלא והן את אנטיגן ה-STV בלבד, וכן את אנטיגן ה-STV מעורבב עם משפר CpG.
לאחר תקופה של 70 יום, גילו המדענים כי עכברים שחוסנו בקומפלקס החיסון המלא הפגינו תגובה חיסונית חזקה פי 9 מזו שנגרמה על ידי תערובת CpG/STV. התגובה הבולטת ביותר החלה על ידי המבנה הטטרהדרלי (פירמידלי). עם זאת, התגובה החיסונית לקומפלקס החיסון זוהתה לא רק כספציפית (כלומר, תגובת הגוף לאנטיגן ספציפי בו השתמשו הנסיינים) ויעילה, אלא גם כבטוחה, דבר שאושר על ידי היעדר תגובה חיסונית ל-DNA "ריק" (שאינו נושא ביומולקולות) שהוכנס לתאים.
"היינו מרוצים מאוד", אומר צ'אנג. "זה היה נפלא לראות תוצאות שחזינו. זה לא קורה לעתים קרובות בביולוגיה."
עתיד תעשיית התרופות טמון בתרופות ממוקדות
כעת הצוות בוחן את הפוטנציאל של שיטה חדשה לגירוי תאי חיסון ספציפיים לעורר תגובה באמצעות פלטפורמת DNA. הטכנולוגיה החדשה יכולה לשמש ליצירת חיסונים המורכבים ממספר תרופות פעילות, וכן לשינוי מטרות כדי לווסת את התגובה החיסונית.
בנוסף, לטכנולוגיה החדשה יש פוטנציאל לפתח שיטות חדשות לטיפול ממוקד, ובפרט ייצור של תרופות "ממוקדות" המועברות לאזורים ספציפיים בגוף ולכן אינן מייצרות תופעות לוואי מסוכנות.
לבסוף, למרות שתחום ה-DNA עדיין בחיתוליו, לעבודתם המדעית של חוקרי אריזונה יש השלכות מעשיות משמעותיות על רפואה, אלקטרוניקה ותחומים אחרים.
צ'אנג ויאנג מודים שעדיין יש הרבה מה ללמוד ולמטב לגבי שיטת החיסון שלהם, אך ערך התגלית שלהם אינו ניתן להכחשה. "עם הוכחת היתכנות ביד, אנו יכולים כעת לייצר חיסונים סינתטיים עם מספר בלתי מוגבל של אנטיגנים", מסכם צ'אנג.
תמיכה כספית למחקר זה ניתנה על ידי משרד ההגנה האמריקאי והמכונים הלאומיים לבריאות.
 [ 1 ], [ 2 ], [ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ]
[ 1 ], [ 2 ], [ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ]

